وقد أظهرت الدراسات أن العلاج بالأكسجين عالي الضغط (HBOT) يحسن وظائف القلب بشكل رئيسي عن طريق الحد من الإجهاد الأكسجين ، وتنظيم استقلاب الطاقة وتثبيط الخلايا المبرمج.
يتم تقييم التأثيرات الوقائية للقلب من HBOT بشكل رئيسي من قبل إليسا ، ومسابير الفلورسنت ، والميكروسكوب الإلكتروني الناقل والنسخ العكسي-PCR الكمي (RT-qPCR).
كما لوحظ مع المجهر الإلكتروني انتقال ، وذلك باستخدام 0.25MPa غرفة الضغط العالي ل HBOT لمدة 14 يوما (مرة واحدة في اليوم) قد تحسنت التشكل الميتوكوندريا وتقليل عدد من الحويصلات الذاتية.
HBOT زاد بشكل كبير مستويات فتح ATP و ADP وشحن الطاقة ونفاذية الميتوكوندريا المسام الانتقالية ، ولكن انخفض مستويات أمبير ، السيتوكروم ج وأنواع الأكسجين التفاعلية ، التي تم تحديدها باستخدام RT qPCR أو الكيمياء المناعية. بالإضافة إلى ذلك ، زاد HBOT بشكل كبير من مستويات التعبير الجيني أو البروتين لبروتين الربط eIF4E 1 ، الهدف الثديي للراباميسين (mTOR) ، الميتوكوندريا ، الوحدة الفرعية 1 لديهيدروجيناز NADH ، mitofusin 1 و mitofusin 2 ، مع انخفاض مستويات التعبير الجيني أو البروتين للبلعمة الذاتية 5 (Atg5) ، والسيتوكروم سي ، والبروتين المرتبط بالحركية 1 ، أو p53.
يتم التعبير عن البيانات على أنها المتوسط ± SD (n = 5). * P {من ؟ ؟ ؟ ؟ ؟ ؟ ؟ ؟ ؟ ؟ ؟ ؟ ؟
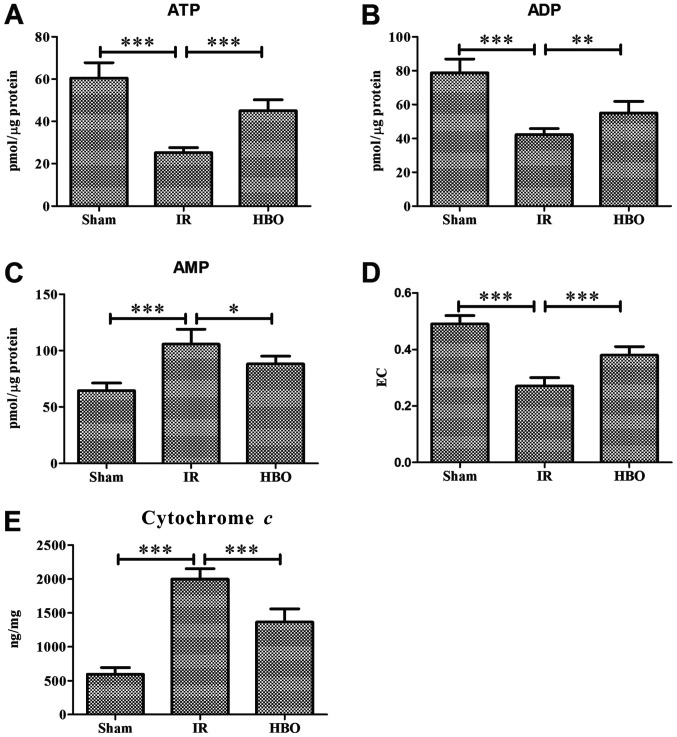
(عبد) يتم تحديد ATP ، ADP ، EC في مجموعة الشام ، مجموعة الأشعة تحت الحمراء ومجموعة HBO.
(CE) استخدم مجموعة إليسا للكشف عن مجموعة الشام ومجموعة الأشعة تحت الحمراء ومجموعة HBO
HBO ، الأكسجين عالي الضغط ؛ EC ، شحن الطاقة ؛ IR ، ischemia/reperfusion.
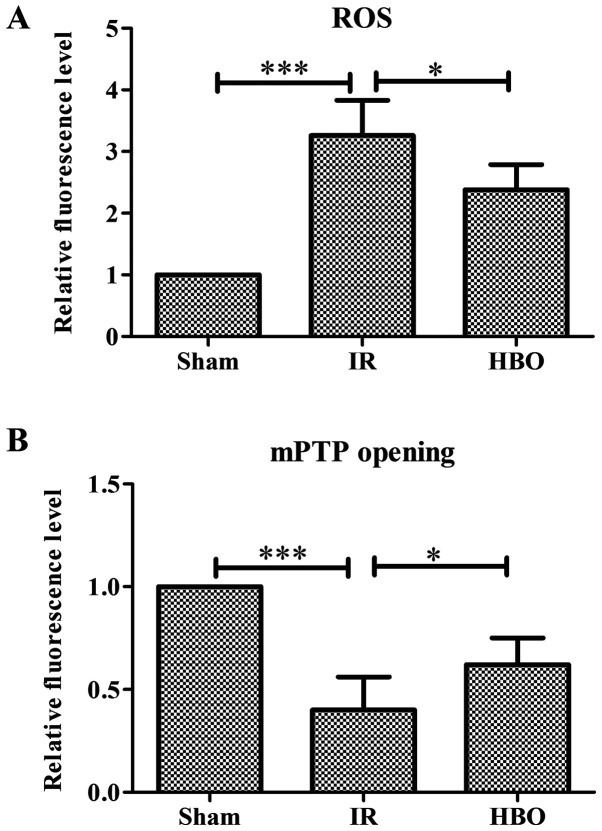
HBO ، الأكسجين عالي الضغط ؛ ROS ، أنواع الأكسجين التفاعلية ؛ mPTP ، نفاذية الميتوكوندريا المسام الانتقالية ؛ IR ، الإسكيمية/إعادة الانصهار ؛ DHE ، ثنائي هيدروإيثيديوم.
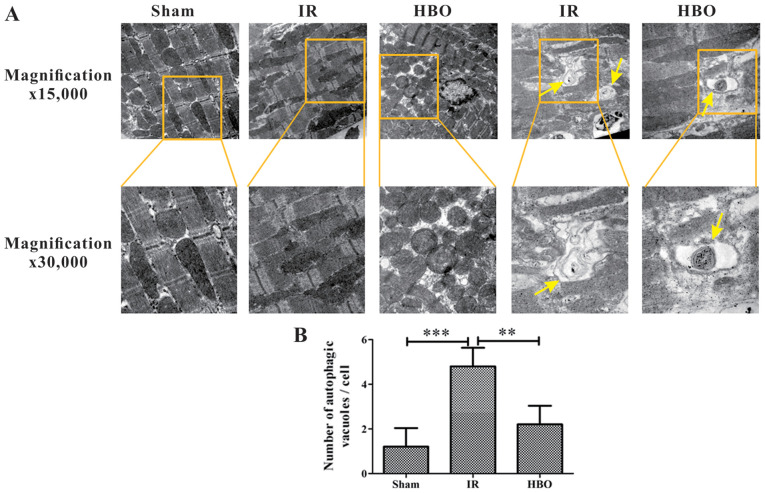
(أ) تصوير مصور تمثيلي لأنسجة عضلة القلب في المجموعة الزائفة ، ومجموعة الأشعة تحت الحمراء ومجموعة HBO. كانت الميتوكوندريا في المجموعة الزائفة طبيعية ، ولم تلاحظ أي حويصلات ذاتية المفعول. بالمقارنة مع المجموعة الزائفة ، لوحظت أضرار كبيرة للميتوكوندريا وزيادة في عدد الفراغات الذاتية في مجموعة الأشعة تحت الحمراء. مقارنة مع مجموعة الأشعة تحت الحمراء ، لوحظت أضرار طفيفة فقط في الميتوكوندريا وانخفاض في عدد الحويصلات الذاتية (تغييرات دائرة متحدة المركز) في مجموعة HBO. السهام الصفراء تشير الحويصلات الذاتية.
(ب) شبه كمي لعدد الحويصلات الذاتية في مجموعة الشام ومجموعة الأشعة تحت الحمراء ومجموعة HBO (n = 5).
إر ، الإسكيمية/ريبيرفيوجن ؛ هبو ،الأكسجين عالي الضغط.
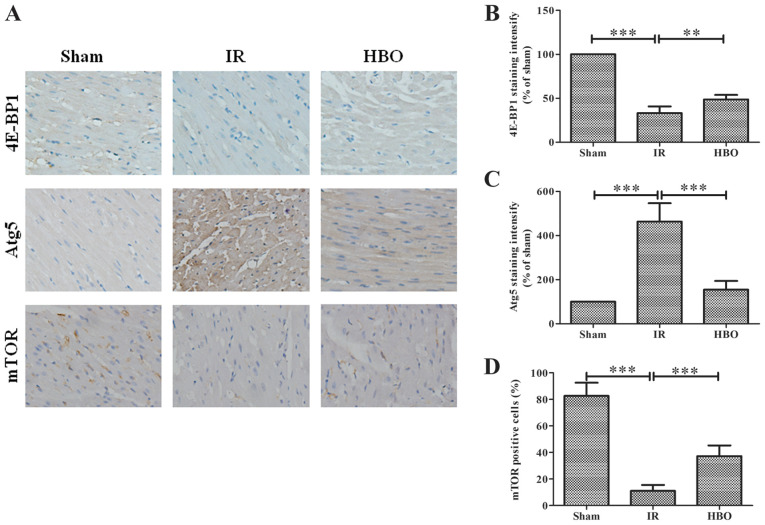
(أ) تلطيخ عضلي مناعي كيميائي للكشف عن مستويات التعبير من 4E-BP1 ، Atg5 ومتور في مجموعة الشام ، ومجموعة الأشعة تحت الحمراء ومجموعة HBO. كانت النواة ملطخة باللون الأزرق ، وكان البروتين المستهدف ملطخ باللون البني.
شبه كمي لمستويات تعبير mTOR (B) 4E-BP1 و (C) Atg5 و (D) في مجموعة الشام ومجموعة IR ومجموعة HBO. يتم تطبيع البيانات إلى المجموعة الزائفة ويعبر عنها بنسب مئوية.
الأشعة تحت الحمراء ، الإسكيمية/إعادة ضخ. HBO ، الأكسجين عالي الضغط. Atg5 ، ذات الصلة بالبلعمة الذاتية 5 ؛ 4E-BP1 ، عامل البدء في حقيقيات النواة بروتين ملزم 4E 1 ؛ mTOR ، الهدف الثديي للراباميسين.
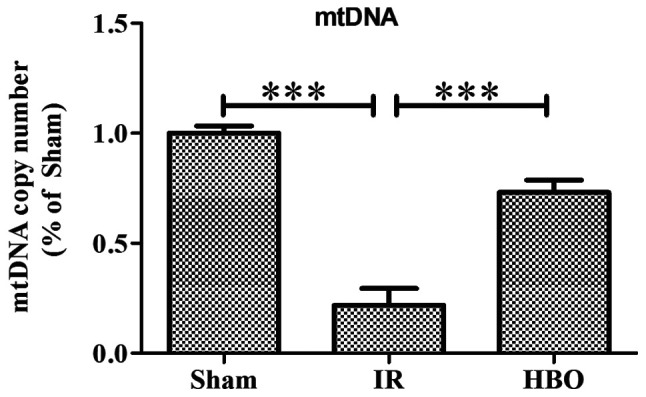
يتم تطبيع البيانات إلى المجموعة الزائفة ويعبر عنها بنسب مئوية. MtDNA ، mitochondrial DNA.
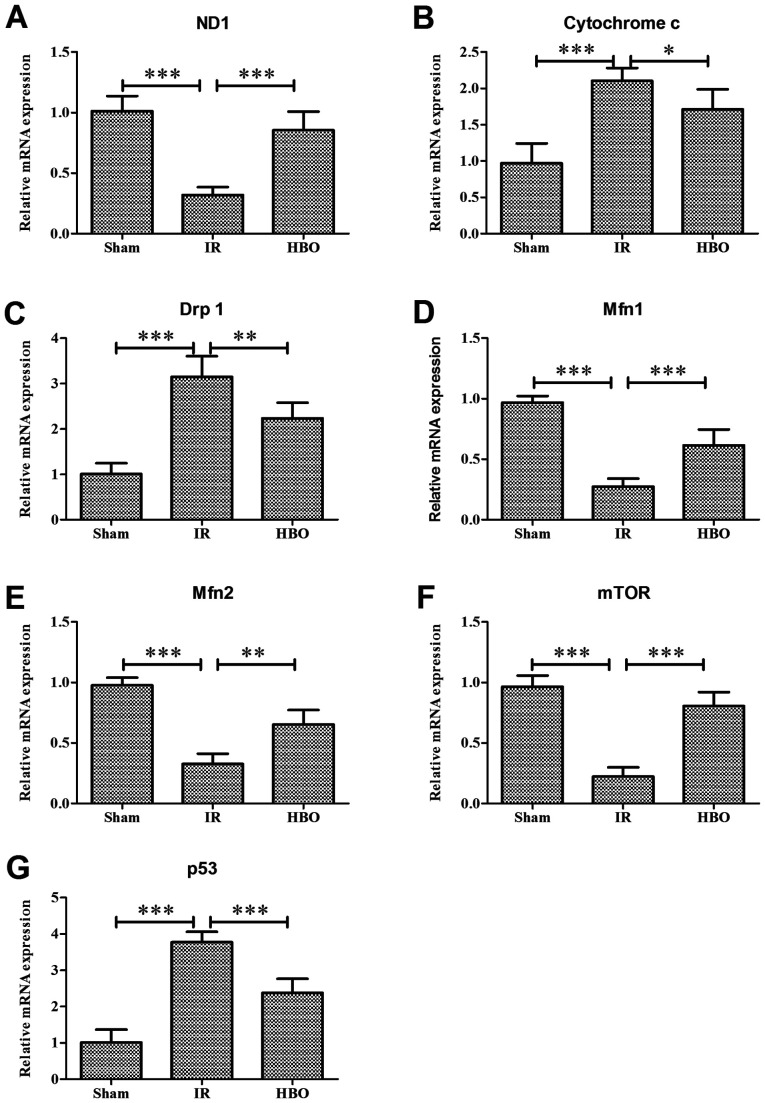
(AE) تأثير المعالجة المسبقة لـ HBO على مستويات تعبير mRNA في الجينات المرتبطة بديناميات الميتوكوندريا: (A) ND1, (B) السيتوكروم c, (C) Drp1, (D) mfn1 و (E) Mfn2 في مجموعة الشام ومجموعة الأشعة تحت الحمراء ومجموعة HBO.
تأثير HBOT على مستوى التعبير للجينات المرتبطة بالبلعمة الذاتية: (F) mTOR و (G) p53 كانتا في مجموعة shame و IR و HBO.
HBO ، الأكسجين عالي الضغط ؛ IR ، ischemia/repermusion ؛ ND1 ، NADH dehyrogenase subunit 1 ؛ Drp1 ، dynein ذات الصلة البروتين 1 ؛ mitofusin 1 ؛ Mfn2 ، mitofusin 2.
باختصار ، فقد لوحظ أن العلاج HBOT يحمي خلايا القلب أثناء الإصابة بنقص التروية القلبي (ميري) عن طريق منع ضعف الميتوكوندريا وتثبيط الالتهام الذاتي.
لذلك ، توفر هذه النتائج أدلة جديدة لدعم استخدام HBOT كطريقة محتملة للتخفيف من حدة الميري.
كر: من أجل